§4. Свойства и функции белков
«Белки химия» - В состав слизи и синовиальной жидкости входят мукопротеиды. Структура белка. Кожа и волосы защищают внутреннюю среду организма от внешних воздействий. 2) Денатурация. Белки. Такие аминокислоты называются незаменимыми. Определение. Метионин лизин аргинин аспарагин аспарагиновая кислота глутаминовая кислота.
«Белка и Стрелка» - Белка и Стрелка первые космонавты. Стрелка в Музее Космонавтики. Через некоторое время у Стрелки появились щенки. Белка - беспородная самка белого окраса - была самая активная и общительная. Одними из наиболее приспособившихся собак-претендентов были Белка и Стрелка. 19 августа 1960 года был совершён успешный запуск космического корабля-спутника на орбиту.
«Урок Белки» - Конспект урока. Развивающая: развитие умения анализировать, сравнивать, делать выводы о свойствах белков. Белки. Уровни организации белковой молекулы. Рождение урока начинается: Почему молекулы аминокислот могут взаимодействовать между собой? Качественные реакции белков: биуретовая; ксантопротеиновая; реакция определения серы в белках.
«Дети с нарушением слуха» - Циолковский первым разработал модель ракеты, способной полететь в космос. Отставание мыслительной деятельности слабослышащих детей: С возникновением новых форм мышления старые формы не только не исчезают, а сохраняются и развиваются. Дети сравнительно поздно начинают осознавать свой дефект, как препятствие к развитию.
«Жиры белки углеводы» - Углеводы, как и жиры, являются энергетическим материалом. Что же такое рациональное питание? Проблема. Обед: макароны с сыром 430Ккал. Белки называют еще носителями жизни. Вывод. Результат. Наше питание. Задача. Узнать, почему необходимо правильно питаться и во время, чтобы не заболеть. От правильного питания будет зависить повышенность или пониженность нашего иммунитета.
«Белки урок» - Общие свойства белков. Структура белковой молекулы. Функции белков. Содержание белков в организме (в процентах к сухой массе). Качественные реакции. Что такое жизнь? Биуретовая Ксантопротеиновая HNO3 NaOH CuSO4. Белки. Содержание белков в пище. Четвертичная структура белковой молекулы.
Среди органических веществ белки , или протеины , - самые многочисленные, наиболее разнообразные и имеющие первостепенное значение биополимеры. На их долю приходится 50 - 80% сухой массы клетки.
Молекулы белков имеют большие размеры, поэтому их называют макромолекулами . Кроме углерода , кислорода , водорода и азота , в состав белков могут входить сера, фосфор и железо. Белки отличаются друг от друга числом (от ста до нескольких тысяч), составом и последовательностью мономеров. Мономерами белков являются аминокислоты (рис. 1)
Бесконечное разнообразие белков создается за счет различного сочетания всего 20 аминокислот. Каждая аминокислота имеет свое название, особое строение и свойства. Их общую формулу можно представить в следующем виде:
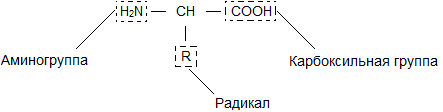
Молекула аминокислоты состоит из двух одинаковых для всех аминокислот частей, одна из которых является аминогруппой (-NH 2 ) с основными свойствами, другая - карбоксильной группой (-COOH ) с кислотными свойствами. Часть молекулы, называемая радикалом (R ), у разных аминокислот имеет различное строение. Наличие в одной молекуле аминокислоты основной и кислотной групп обусловливает их высокую реакционную способность. через эти группы происходит соединение аминокислот при образовании белка. При этом возникает молекула воды, а освободившиеся электроны образуют пептидную связь. Поэтому белки называют полипептидами .
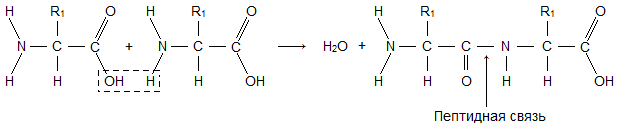
Молекулы белков могут иметь различные пространственные конфигурации, и в их строении различают четыре уровня структурной организации.
Последовательность аминокислот в составе полипептидной цепи представляет первичную структуру
белка. Она уникальна для любого белка и определяет его форму, свойства и функции.
Большинство белков имеют вид спирали в результате образования водородных связей между -CO-
и -NH-
группами разных аминокислотных остатков полипептидной цепи. Водородные связи малопрочные, но в комплексе они обеспечивают довольно прочную структуру. Эта спираль - вторичная структура
белка.
Третичная структура - трехмерная пространственная «упаковка» полипептидной цепи. В результате возникает причудливая, но для каждого белка специфическая конфигурация - глобула . Прочность третичной структуры обеспечивается разнообразными связями, возникающими между радикалами аминокислот.
Четвертичная структура
характерна не для всех белков. Она возникает в результате соединения нескольких макромолекул с третичной структурой в сложный комплекс. Например, гемоглобин крови человека представляет комплекс из четырех макромолекул белка.
Такая сложность структуры белковых молекул связана с разнообразием функций, свойственных этим биополимерам.
Нарушение природной структуры белка называют денатурацией
. Она может происходить под воздействием температуры, химических веществ, лучистой энергии и других факторов. При слабом воздействии распадается только четвертичная структура, при более сильном - третичная, а затем - вторичная, и белок остается в виде полипептидной цепи.
Этот процесс частично обратим: если не нарушена первичная структура, то денатурированный белок способен восстанавливать свою структуру. Отсюда следует, что все особенность строение макромолекулы белка определяются его первичной структурой.
Кроме простых белков , состоящих только из аминокислот, есть еще и сложные белки
Классификация белков. По форме молекул белки можно разделить на две большие группы – глобулярные (имеют сферическую форму) и фибриллярные (удлиненной формы). Так, глобулярными белками являются глобулины и альбумины крови, фибриноген, гемоглобин. Фибриллярные белки – кератин, коллаген, миозин и др. (рис.)
Белки, образованные только аминокислотами, называются простыми . Сложными являются белки, имеющие в своем составе компонент неаминокислотной природы. Это могут быть ионы металлов (Fe, Zn, Mg, Mn), липиды, нуклеотиды, сахара и др. Простыми белками являются сывороточный альбумин крови, фибрин, некоторые ферменты (трипсин) и др. Сложными белками являются липопротеины и гликопротеины (например, иммуноглобулины), а также большинство ферментов.
Денатурация и ренатурация белков . Одно из основных свойств белков - способность изменять свою структуру и свойства под влиянием различных факторов (действие концентрированных кислот и щелочей, высокая температура и др.). Процесс нарушения природной конформации белков под влиянием каких-либо факторов без нарушения первичной структуры называется денатурацией (от лат. де - приставка, означающая потерю, и натура - природные свойства) (рис.). Изменение структуры белка происходит вследствие разрыва водородных и ионных связей, стабилизирующих пространственные структуры. При денатурации могут утрачиваться четвертичная, третичная и даже вторичная структура. Денатурация сопровождается потерей биологической активности белка. При этом наблюдается уменьшение растворимости белка, изменение формы и размеров молекул, потеря ферментативной активности и т.д. Денатурирующими агентами являются: высокая температура, кислоты и щелочи, мочевина, спирты, фенол, хлорамин, соли тяжелых металлов и др. Так, соли тяжелых металлов (кадмия, ртути и др.) при взаимодействии с белками образуют нерастворимые соединения, и белки выпадают в осадок.
Как правило, денатурация имеет необратимый характер. Хотя на первых ее стадиях, при условии прекращения действия повреждающих факторов, белок может восстановить свое первоначальное состояние. Это явление называется ренатурацией (от лат. ре - приставка, обозначающая возобновление). В организмах обычно наблюдается частичная обратимая денатурация белков.
Способность белков к обратимому изменению своей структуры в ответ на действие физических и химических факторов лежит в основе важнейшего свойства всех живых систем - раздражимости .
Под влиянием некоторых факторов (воздействие формалина, спирта, щелочей и др.) может происходит разрушение первичной структуры. Процесс разрушения первичной структуры белков, называемый деструкцией (от лат. де - и структура - строение), всегда необратимый.
Явление денатурации часто используется в биологических исследованиях и в медицине. При определении в биологическом материале низкомолекулярных соединений из раствора сначала удаляют белки. Для этого вызывают их денатурацию, осаждают или отфильтровывают.
В медицине денатурирующие агенты часто применяются для стерилизации медицинских инструментов и материалов в автоклавах (здесь денатурирующий агент – высокая температура). Их используют также в качестве антисептиков (спирт, фенол, хлорамин и др.) для очистки загрязненных материалов и поверхностей. То же происходит при обеззараживании ран, ссадин, царапин раствором йода или спиртом. На денатурации белков основано применение мышьяковистого ангидрида в стоматологической практике при лечении пульпита.
Функции белков. Большое разнообразие белков позволяет им выполнять в живом организме множество различных функций, как структурных, так и метаболических.
Структурная. Белки входят в состав всех биологических мембран и органоидов клетки. Преимущественно из белков состоят хрящи, сухожилия. В их состав входит белок коллаген . Кератин – компонент перьев, волос, ногтей, когтей, рогов, копыт у высших животных. Эластин является компонентом связок, стенок кровеносных сосудов.
Каталитическая (ферментативная). Белковые молекулы ферментов способны ускорять течение биохимических реакций в клетках живых организмов в сотни миллионов раз. Ферменты участвуют как в процессах синтеза, так и распада веществ. Они обеспечивают расщепление питательных веществ в пищеварительном тракте, фиксацию углерода при фотосинтезе и т.д.
Механизм действия ферментов объясняет теория активного центра . Согласно ей, в молекуле каждого фермента имеется один или более участков, в которых происходит тесный контакт между молекулами фермента и специфического вещества - субстрата (рис.). Активным центром выступает функциональная группа (например, ОН-группа серина), отдельная аминокислота либо сочетание нескольких (в среднем от 3 до 12), расположенных в определенном порядке аминокислотных остатков. Форма и химическое строение активного центра таковы, что с ним могут связываться только определенные субстраты в силу точного соответствия их пространственных структур (как ключ и замок).
Молекула фермента вызывает ослабление определенных химических связей субстрата, и катализируемая реакция происходит с меньшими начальными затратами энергии, а следовательно, с намного большей скоростью. Ферменты ускоряют ход реакции без изменения ее общего результата за счет снижения энергии активации , т.е. в их присутствии затрачивается значительно меньше энергии для придания молекулам реакционной способности.
На заключительном этапе химической реакции фермент-субстратный комплекс распадается с образованием конечных продуктов и свободного фермента, который сохраняет исходную структуру и свойства. Освободившийся при этом активный центр может принимать следующие новые молекулы субстрата. Именно поэтому ферменты требуются в крайне низких концентрациях.
Некоторые ферменты, помимо активного центра, имеют один или несколько регуляторных центров. С этими участками могут связываться молекулы, регулирующие активность фермента. Они носят название активаторов (от лат. активус - деятельностный).
Молекулы некоторых веществ, взаимодействуя с ферментом, снижают или блокируют его активность (рис.). Такие вещества называются ингибиторами (от лат. ингибео – сдерживаю, останавливаю) . Например, многие лекарственные препараты природного или синтетического происхождения являются ингибиторами определенных ферментов. Кроме того, в основе действия некоторых токсических веществ лежит ингибирование активного центра ферментов.
Транспортная. Многие белки способны присоединять и переносить различные вещества. Гемоглобин связывает и переносит кислород и углекислый газ. Альбумины крови транспортируют жирные кислоты, глобулины - ионы металлов и гормоны. Молекулы белков, входящие в состав цитоплазматической мембраны, принимают участие в транспорте веществ в клетку и из нее.
Сократительная (или двигательная). Сократительные белки обеспечивают способность клеток, тканей, органов и целых организмов изменять форму, двигаться. Так, актин и миозин – обеспечивают работу мышц и немышечные внутриклеточные сокращения. Белок тубулин входит в состав микротрубочек веретена деления, ресничек и жгутиков эукариотических клеток.
Регуляторная . Некоторые пептиды и белки являются гормонами. Они влияют на различные физиологические процессы. Например, инсулин регулирует содержание глюкозы в крови. Глюкагон регулирует расщепление гликогена до глюкозы, повышая ее содержание в крови.
Сигнальная. Некоторые белки клеточных мембран способны изменять свою структуру в ответ на действие факторов внешней среды. Так происходит прием сигналов из внешней среды и передача информации в клетку. Примером может служить фитохром - светочувствительный белок, регулирующий фотопериодическую реакцию растений, и onсин - составная часть пигмента родопсина, находящегося в клетках сетчатки глаза.
Защитная. Специфические белки предохраняют организм от вторжения чужеродных организмов и от повреждений. Так в ответ на проникновение чужеродных тел - антигенов - в клетке вырабатываются антитела - особые белки, называемые иммуноглобулинами, которые обеспечивают иммунитет. Интерфероны защищают организм от вирусной инфекции. Фибриноген , тромбопластин и тромбин участвуют в свертывании крови и предотвращении кровопотери.
Токсическая. Многие живые существа в качестве собственной защиты выделяют белки, называемые токсинами , которые в большинстве случаев являются ядами для других организмов. Токсины синтезируются в организме некоторых змей, лягушек, насекомых, грибов, растений, бактерий. В свою очередь, некоторые организмы способны вырабатывать антитоксины , которые подавляют действие этих ядов.
Энергетическая. Белки могут служить источником энергии в клетке (после гидролиза). При полном окислении 1 г белка выделяется 17,6 кДж энергии. Белки расходуются на энергетические нужды в крайних случаях, когда исчерпаны запасы углеводов и жиров.
С белками могут взаимодействовать некоторые вещества и подавлять их функции. Такие вещества называются ингибиторами. Ингибиторами белковых функций являются многие яды. Так, например, ингибиторами белков-рецепторов постсинаптической мембраны, которые связываются с медиатором ацетилхолином при передаче нервного импульса в синапсах, являются мускарин (токсин мукора) и никотин . При этом нарушается проведение нервного импульса. Подобное действие оказывает также атропин – вещество, содержащееся в растениях красавки и белены. Атропин является ингибитором М-холинорецепторов. Учитывая, что связывание ацетилхолина с М-холинорецепторами вызывает сокращение многих гладких мышц, атропин используется как лекарственное средство, снимающее их спазм (спазмолитик). Однако при передозировке атропином могут наблюдаться двигательное и психическое возбуждение, галлюцинации, признаки понижения тонуса гладких мышц радужной оболочки глаз, бронхов, органов брюшной полости. Такой же эффект наблюдается при употреблении отваров белены (отсюда поговорка «белены объелся».
s1. Что общего и чем отличаются процессы денатурации и деструкции? 2. Чем обусловлено разнообразие свойств белков? 3 . Каковы основные биологические функции белков? 4. В чем состоит защитная функция белков? 5. Чем определяется двигательная функция белков? 6. Что такое ферменты? Почему без участия ферментов протекание большинства биохимических процессов в клетке было бы невозможным?
Важное свойство белков - их способность к денатурации. Этим понятием обозначают явления, связанные с необратимым изменением вторичной, третичной и четвертичной структур белка под воздействием нагревания, кислот, щелочей, УФ-лучей, ионизирующей радиации, ультразвука и др. Иными словами, денатурация - это необратимое нарушение нативной пространственной конфигурации белковой молекулы, сопровождающееся существенными изменениями биологических и-физико-химических свойств белков.
Поскольку в образовании вторичной и третичной структур частично участвуют относительно слабые связи, физическое состояние белка в значительной степени зависит от температуры, рН, присутствия солей и других факторов. Нагревание, например, вызывает распрямление полипептидной цепи белковой молекулы; некоторые химические реагенты разрывают водородные связи. Изменение рН также обусловливает разрыв связей, при этом проявляется электростатическая неустойчивость.
Белки под влиянием различных физических и химических факторов теряют свои первоначальные (нативные) свойства. Внешне это выражается в их свертывании и выпадении в осадок. Примером такого явления может служить свертывание альбумина молока при кипячении. Негидролитическое необратимое нарушение нативной структуры белка и называется денатурацией. При этом рвутся в основном водородные связи, изменяется пространственная структура белка, однако разрыва ковалентных связей в белковой молекуле не происходит.
Денатурация приводит к развертыванию молекулы белка, и он переходит в более или менее разупорядоченное состояние (в нем уже нет ни спиралей, ни слоев, ни других каких-либо видов регулярной укладки цепи). В денатурированном состоянии амидные группы пептидной цепи образуют водородные связи с окружающими их молекулами воды; таких водородных связей значительно больше, чем внутримолекулярных.
Взбивание яичного белка, сливок превращает их в пену, состоящую из пузырьков воздуха, окруженных тонкими белковыми пленками, образование которых сопровождается развертыванием полипептидных цепей в результате разрыва связей при механическом воздействии. Таким образом, при образовании пленок происходит частичная или полная денатурация белка. Такой вид денатурации называется поверхностной денатурацией белка.
Для кулинарных процессов особое значение имеет тепловая денатурация белков. Механизм тепловой денатурации белков можно рассмотреть на примере глобулярных белков.
Основная молекула глобулярного белка состоит из одной или нескольких полипептидных цепей, сложенных складками и образующих клубки. Такая структура стабилизируется непрочными связями, среди которых большую роль играют водородные связи, образующие поперечные мостики между параллельными пептидными цепями или их складками.
При нагревании белков начинается усиленное движение полипептидных цепей или складок, что приводит к разрыву непрочных связей между ними. Белок разворачивается и приобретает необычную, неприродную форму, водородные и другие связи устанавливаются в несвойственных данной молекуле местах, и конфигурация молекулы меняется. В результате происходит развертывание и перегруппировка складок, сопровождаемые перераспределением полярных и неполярных групп, причем неполярные радикалы концентрируются на поверхности глобул, понижая их гидрофильность. При денатурации белки становятся нерастворимыми и в большей или меньшей мере утрачивают способность к набуханию.
При тепловой денатурации белков активная роль принадлежит воде, которая участвует в образовании новой конформационной структуры денатурированного белка. Полностью обезвоженные белки не денатурируют даже при длительном нагревании. Денатурирующий эффект внешних воздействий тем сильнее, чем выше гидратация белков и ниже их концентрация в растворе.
При значениях рН среды, близких к ИЭТ белка, происходит максимальная дегидратация белка. Наиболее полно денатурация осуществляется в ИЭТ белка. Смещение рН в ту или иную сторону от ИЭТ белка способствует повышению его термостабильности и ослаблению денатурационных процессов.
Температура денатурации белков повышается в присутствии других термостабильных белков и некоторых веществ небелковой природы, например сахарозы. Это свойство белков используют, когда при тепловой обработке необходимо повышение температуры смеси (например, при пастеризации мороженого, изготовлении яично-масляных кремов), не допуская расслоения или структурообразования в белковой коллоидной системе.
Появление на поверхности белковой молекулы после денатурации ранее скрытых радикалов или функциональных групп изменяет физико-химические и биологические свойства белков. В результате денатурации свойства белков необратимо изменяются.
Из прогретой муки нельзя приготовить тесто, а из вареного мяса - котлеты, так как денатурированные белки не обладают способностью к гидратации и образованию вязких упруго-пластичных масс, пригодных для формования полуфабрикатов.
Потеря способности к гидратации объясняется утратой белками нативных свойств, важнейшим из которых является выраженная гидрофильность (большое сродство к воде), и связана с изменением конформации полипептидных цепей в белковой молекуле в результате денатурации.
Набухание и растворимость белков в воде обусловлены наличием на поверхности белковых молекул большого числа гидрофильных групп (СООН, ОН, NH 2), способных связывать значительное количество воды.
Как уже отмечалось, способность разных нативных белков пищевых продуктов растворяться в каком-либо растворителе (воде, растворах нейтральных солей, слабых растворах щелочей, спирте и др.) используют для разделения или выделения определенной белковой фракции (для исследовательских или пищевых целей). Денатурированные белки такими различиями не обладают, они все одинаково нерастворимы и не способны набухать в воде. Исключение из этого общего правила составляет фибриллярный коллаген мяса и рыбы, который после тепловой денатурации и деструкции до глютина способен растворяться в горячей воде.
В результате денатурации белки теряют биологическую активность. В растительном и животном сырье, используемом на предприятиях общественного питания, активность большинства белковых веществ сохраняется. Так, в результате деятельности ферментов плоды при хранении дозревают (а иногда и перезревают), картофель и корнеплоды прорастают. Особенно наглядно деятельность ферментов проявляется в клубнях картофеля при хранении их на свету: поверхность клубней приобретает зеленую окраску и горький вкус соответственно в результате синтеза хлорофилла и образования ядовитого гликозида соланина.
В сыром мясе тканевые ферменты также находятся в активном состоянии, участвуя в автолизе мяса (послеубойном созревании). Это их свойство используют для практических целей. Полная инактивация кислой фосфатазы происходит при достижении температуры в геометрическом центре мясного изделия 80 "С, что соответствует температуре пастеризации (отмиранию вегетативных форм бактерий). При необходимости проверить достаточность тепловой кулинарной обработки мясного изделия определяют наличие или отсутствие в нем активной кислой фосфатазы.
В нативном белке пептидные группы экранированы внешней гидратной оболочкой или находятся внутри белковой глобулы и таким образом защищены от внешних воздействий. При денатурации белок теряет гидратную оболочку, что облегчает доступ пищеварительным ферментам желудочно-кишечного тракта к функциональным группам. Белок переваривается быстрее.
Кроме того, иногда ингибиторная функция белка исчезает после денатурации. Так, некоторые белки яйца отрицательно влияют на процесс пищеварения: авидин в кишечнике связывает биотин (витамин Н), который участвует в регуляции нервной системы и нервно-рефлекторной деятельности; овомукоид угнетает действие трипсина (фермента поджелудочной железы). Именно поэтому белки сырого яйца не только плохо перевариваются, но и частично всасываются в непереваренном виде, что может вызвать аллергию, уменьшить усвояемость других компонентов пищи и ухудшить всасывание соединений кальция. При денатурации эти белки утрачивают свои антиферментные свойства.
При денатурации белок теряет гидратную оболочку, в результате чего многие функциональные группы и пептидные связи белковой молекулы оказываются на поверхности и белок становится более реакционноспособным.
В результате тепловой денатурации белка происходит агрегирование белковых молекул. Поскольку гидратная оболочка вокруг молекулы белка нарушается, отдельные молекулы белка соединяются между собой в более крупные частицы и уже не могут держаться в растворе. Начинается процесс свертывания белков, в результате которого образуются новые молекулярные связи.
Взаимодействие денатурированных молекул белка в растворах и гелях протекает по-разному. В слабоконцентрированных белковых растворах при тепловой денатурации агрегация молекул белка происходит путем образования межмолекулярных связей как прочных, например дисульфидных, так и слабых (но многочисленных) - водородных. В результате образуются крупные частицы. Дальнейшая агрегация частиц приводит к расслоению коллоидной системы, образованию хлопьев белка, выпадающих в осадок или всплывающих на поверхность жидкости, часто с образованием пены (например, выпадение в осадок хлопьев денатурированного лактоальбумина при кипячении молока; образование хлопьев и пены из денатурирующих белков на поверхности мясных и рыбных бульонов). Концентрация белков в таких растворах не превышает 1 %.
В более концентрированных белковых растворах при денатурации белков образуется сплошной гель, удерживающий всю воду, содержащуюся в коллоидной системе. В результате агрегации денатурированных молекул белка образуется структурированная белковая система. Денатурация белков в концентрированных растворах с образованием сплошного геля происходит при тепловой обработке мяса, рыбы (белки саркоплазмы), куриных яиц и разных смесей на их основе. Точные концентрации белков, при которых их растворы в результате нагревания образуют сплошной гель, неизвестны. Учитывая, что способность к гелеобразованию у белков зависит от конфигурации (асимметрии) молекул и характера образующихся при этом межмолекулярных связей, надо полагать, что для разных белков указанные концентрации различны.
Например, для приготовления омлетов к яичному меланжу добавляют 38...75 % молока. Нижние пределы относятся к омлетам жареным, верхние - к вареным на пару. Для приготовления омлетов из яичного белка, используемых в диетическом питании, молоко добавляют в количестве 40 % независимо от способа тепловой обработки, так как в белке яйца концентрация белков значительно ниже, чем в желтке.
Некоторые белки, представляющие собой более или менее обводненные гели, при денатурации уплотняются, в результате чего происходит их дегидратация с отделением жидкости в окружающую среду. Белковый гель, подвергшийся нагреванию, как правило, характеризуется меньшим объемом, массой, пластичностью, повышенной механической прочностью и большей упругостью по сравнению с исходным гелем нативных белков. Подобные изменения белков наблюдаются при тепловой обработке мяса, рыбы (белки миофибрилл), варке круп, бобовых, макаронных изделий, выпечке изделий из теста.
Гелями и студнями называются твердообразные нетекучие структурированные системы, образовавшиеся в результате действия молекулярных сил сцепления между коллоидными частицами или макромолекулами полимеров. Ячейки пространственных сеток гелей и студней обычно заполнены растворителем.
Таким образом, гели представляют собой коллоидные системы или растворы высокомолекулярных соединений (ВМС), утратившие текучесть из-за возникновения в них определенных внутренних структур в виде пространственного сетчатого каркаса, ячейки которого заполнены дисперсионной средой. Поскольку заключенная в ячейках дисперсионная среда при этом теряет свою подвижность, ее называют иммобилизированной.
Гели весьма широко распространены в природе: к ним относятся многие строительные материалы (бетоны, цементы, глинистые суспензии), грунты, некоторые минералы (агат, опал), различные пищевые продукты (мука, тесто, хлеб, желе, мармелад, студень), желатин, каучук, ткани живых организмов и многие другие материалы живой и неживой природы.
В зависимости от концентрации дисперсионной среды гели принято подразделять на лиогели, коагели и ксерогели (аэрогели).
Богатые жидкостью гели, содержащие мало сухого вещества (до 1...2 %), называют диогелями. К типичным диогелям относятся кисель, студень (холодец), простокваша, растворы мыл и др.
Студенистые осадки, получаемые в процессе коагуляции некоторых гидрофобных золей, а также хлопьевидные осадки, образующиеся при высаливании растворов ВМС, называются коагелями. Содержание сухого вещества в коагелях достигает 80 %. Однако очень бедные жидкостью хлопья и микрокристаллические порошки, образующиеся при коагуляции типичных гидрофобных коллоидов (гидрозолей золота, серебра, платины, сульфидов) к коагелям не относятся.
Бедные жидкостью или совсем сухие гели называются ксеро-гелями. Примерами ксерогелей могут служить сухой листовой желатин, столярный клей в плитках, крахмал, каучук. К сложным ксерогелям относят многие пищевые продукты (муку, сухари, печенье). Высокопористые ксерогели называют также аэрогелями, поскольку в них дисперсионной средой служит воздух. К аэрогелям относят многие сорбенты (силикагель), твердые катализаторы химических реакций.
В зависимости от природы дисперсной фазы и по способности к набуханию принято различать гели хрупкие и эластичные. Эластичные гели мы будем называть студнями.